- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Теория абсолютных скоростей реакции
Основное положение теории абсолютных скоростей химических реакций в том, что всякий элементарный химический акт протекает через переходное состояние (активированный комплекс).
При этом какое-то короткое время существует объединенная система (активированный комплекс), энергия которой из-за деформации связей выше энергии исходных молекул:
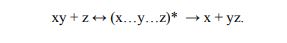
Возникший активированный комплекс существует очень небольшой период времени и находится в равновесии с реагентами.
Затем комплекс распадается с образованием новых молекул – продуктов реакции. Скорость реакции определяется концентрацией активированного комплекса и временем его существования. Потенциальная энергия системы, состоящей из двух сближающихся частиц, меняется и, в принципе, может быть рассчитана, хотя это и непростая задача.
Интересно
Активированный комплекс нельзя рассматривать как молекулу некоторого промежуточного соединения: энергии, длины связей и углы между связями в переходном комплексе искажены и не отвечают средним значениям тех же величин у молекул, на энергетической кривой ему соответствует максимум энергии.
Это вершина потенциального барьера, после которого неизбежно следует понижение энергии. Тем не менее процесс образования активированного комплекса можно (как и обычную реакцию) характеризовать термодинамическими величинами:

Скорость реакции определяется равновесной концентрацией активированного комплекса и константой равновесия процесса Kº∗, выводим кинетическое уравнение бимолекулярной элементарной реакции и выразить ее константу скорости через термодинамические характеристики процесса образования активированного комплекса из исходных молекул:

В основе теории абсолютных скоростей лежит принципиально верная модель химического процесса, которая позволяет рассмотреть особенности его протекания.
Согласно этой модели, начальная конфигурация атомов, координаты которых непрерывно меняются, переходит в конечную через образование некоторой критической для данного процесса промежуточной конфигурации – активированного комплекса.
Такие расчеты интенсивно ведутся, но трудоемкость их сильно возрастает с усложнением конфигурации активированного комплекса. Поэтому для сложных реакций, которые чаще всего и представляют практический интерес, приходится довольствоваться качественными выводами.
Статьи по теме
- Силы внутреннего трения жидкости. Уравнение Ньютона
- Идеальные модели деформирующихся систем
- Основные понятия реологии
- Учение о процессах деформации систем
- Температурная зависимость скорости реакции
- Теория Дебая–Хюккеля
- Растворы электролитов при диссоциации
- Самоассоциация и электрическое экранирование
- Адсорбция как отклонение
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

